Jeśli chodzi o gaz ziemny, nie możesz nie być z nim nieznany, a obecnie żadne gospodarstwo domowe nie może gotować bez niego. Głównym składnikiem gazu ziemnego jest metan, który jest jednym z najprostszych związków węglowodorów. Przyspieszenie rozwoju i wykorzystania metanu jest kluczem do realizacji zielonego i zrównoważonego rozwoju przemysłu energetycznego i chemicznego. Oprócz bezpośredniego zastosowania jako paliwa metan może być również używany jako zasób C1, to znaczy cząsteczki zawierającej atom węgla i może być nadal przekształcany w celu przygotowania chemikaliów o wysokiej wartości, takiej jak metanol, mormalny kwas i tak dalej. Metan można spalić w tlenu, tworząc wodę i dwutlenek węgla. Czy bez spalania można aktywować i przekształcić wiązania węglowodorów cząsteczek metanu w łagodnych warunkach? Odpowiedź brzmi tak! Jest to reakcja „świętego Graala” w dziedzinie katalizy. Reakcje związane z „Świętym Graalem” są często niezwykle trudne, ponieważ mogą być konieczne przeprowadzone w bardzo trudnych warunkach, lub mogą być konieczne przezwyciężenie nieodłącznych trudności reakcji chemicznej, takich jak aktywacja wysoce stabilnych związków, niski plony i niska selektywność. Wyzwania te utrudniają uświadomienie sobie tych reakcji, ale jeśli można je skutecznie osiągnąć, doprowadzą one do znacznych przełomów w badaniach naukowych i zastosowaniach przemysłowych.

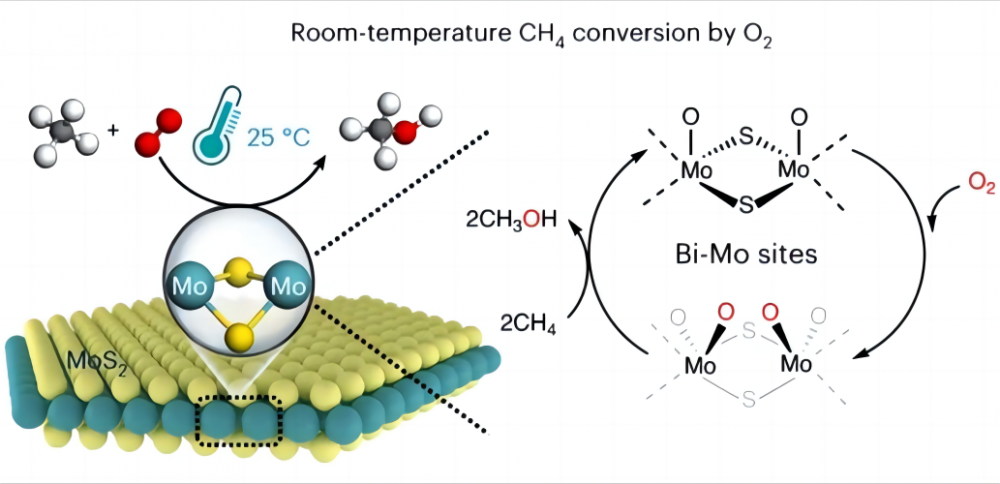
1. Challenges w konwersji metanu w niskich temperaturach Bardzo trudno jest przekształcić metan bezpośrednio na inne przydatne chemikalia z niedrogim tlenem w niskich temperaturach, a nawet temperaturze pokojowej, dlaczego tak jest? Spójrzmy na naturę metanu i tlenu. Struktura chemiczna metanu zawiera cztery identyczne wiązania węglowo-hydrogenowe (CH), które tworzą wysoce symetryczną konfigurację ortotydrowej, a każde wiązanie CH3-H metanu ma energię wiązania do 435 kJ/mol. Możemy myśleć o wiązaniu CH metanu jako szczególnie silnej wiosny. Ta wiosna jest bardzo napięta i wymaga dużej siły do rozciągania. W chemii ta „siła” jest energią wymaganą do zerwania wiązania CH. Ta wysoka energia wiązania sprawia, że wiązania CH metanu termodynamicznie stabilne i bardzo trudne do rozbicia lub reakcji w normalnych warunkach. Z drugiej strony, w reakcjach chemicznych grupy reaktywne są zwykle generowane w ramach interakcji polarnej (interakcja polarna jest zjawiskiem, że cząsteczka ma jeden koniec dodatnio naładowany, a drugi ujemnie naładowany), podczas gdy struktura symetryczna i niepolarna natura cząsteczki metanu zapobiega cząsteczce metanu To z generowania takiej polaryzacji (zgodnie z konfiguracją molekularną, cząsteczka z płaszczyzną symetrii nie ma polaryzacji) i nie może zapewnić grup reaktywnych. Dlatego aktywacja i konwersja metanu jest bardzo trudna i zwykle wymaga trudnych warunków, takich jak wysokie temperatury (600-1100 ° C) lub niektóre „ekstremofile”, takie jak super-odtłuszczone kwasy i wolne rodniki, aby pomóc w aktywacji metanu. Dlatego główna trudność w realizacji aktywacji metanu i tlenu w niskiej temperaturze polega na tym, jak aktywować wiązanie CH metanu, tj. Jak rozciągnąć „sprężynę” w wiązaniu CH. 2. Cud katalizatora Naukowcy wymyślili dobre rozwiązanie tego problemu i postanowili użyć katalizatora, aby pomóc w aktywacji metanu w niskich temperaturach (katalizator jest substancją chemiczną, która nie zmienia się przed reakcją lub po nim, ale przyspiesza reakcję poprzez zmianę minimalnej ilości energii, którą należy wstrzykiwać, aby reakcja miała miejsce). W 2023 r. Kataliza natury dziennika zgłosiła proces osiągania bezpośredniej konwersji metanu z tlenem do tlenków C1 (metanol (CH3OH), kwas mrówkowy (HCOOH) i glikolu metylenowego (HOCH2OH)) przy użyciu specyficznego disulfiku Molybdenum (MOS2) Katalizator w 25 ° C. Konwersję metanu wynoszącą 4,2% i prawie 100% natlenianów C1 osiągnięto przez przekształcenie metanu i tlenu w cenne oksygenaty C1 w warunkach otoczenia. Ten MOS2 jest jedynym zgłoszonym do tej pory katalizatorem, który może zrealizować konwersję metanu i tlenu w temperaturze pokojowej. Wszystko to wynika z unikalnej geometrii i elektronicznej struktury miejsca MO na krawędzi MOS2. To miejsce MO ma wysoką aktywność aktywacyjną w kierunku tlenu w środowisku wodnym, tworząc magiczny gatunek O = mo = O*. Gatunek ten ułatwia złamanie wiązania węglowego i zmniejsza energię aktywacji wiązania CH metanu, zwiększając w ten sposób reaktywność metanu, a tym samym realizację aktywacji metanu i tlenu w niskiej temperaturze. To odkrycie przyniesie więcej możliwości przyszłego wykorzystania energii i ochrony środowiska, a także zapewni nam głębsze zrozumienie niesamowitej roli katalizatorów i pomocników.
3. znaczące strategiczne znaczenie aktywacji metanu w niskiej temperaturze Zdanie bezpośredniej katalitycznej konwersji metanu i tlenu w temperaturze pokojowej oraz przekształcanie metanu w gazu ziemnym w inne przydatne chemikalia, może znacznie poprawić wskaźnik wykorzystania gazu ziemnego, zmniejszyć odpady i lepiej chronić środowisko i uświadomić sobie zrównoważony rozwój energii energii . Po drugie, jako gaz cieplarniany, metan jest drugi po dwutlenku węgla pod względem wkładu w globalne ocieplenie. Jeśli metan można przekształcić w inne substancje, może pomóc nam zmniejszyć emisję zanieczyszczeń powietrza (np. Tlenki węglowe, tlenki azotu, tlenki siarki, węglowodory i związki eterowe) i ułatwić ciśnienie globalnego ocieplenia.




